Différences entre versions de « Dosage acido-basique »
(Page créée avec « {{widget:HautFicheConceptuelle}} {{widget:PBEducation}}<!-- La syntaxe suivante ne doit pas être modifiée--> = {{Widget:Traduction-Fiche}} = Dosage acido basique (... ») |
|||
| (17 versions intermédiaires par le même utilisateur non affichées) | |||
| Ligne 32 : | Ligne 32 : | ||
<!-- Remplacer et adapter le contenu --> | <!-- Remplacer et adapter le contenu --> | ||
| − | [[Fichier: | + | [[Fichier:yyy.jpeg |200 px|Titre de la définition graphique 1]]<!-- Remplacer et adapter le contenu --> |
| − | [[Fichier: | + | [[Fichier:sss.jpeg |200 px|Titre de la définition graphique 2]]<!-- Remplacer et adapter le contenu --> |
| − | [[Fichier: | + | [[Fichier:ttt.gif |200 px|Titre de la définition graphique 3]]<!-- Remplacer et adapter le contenu --> |
{{Widget:Fin-cadre-Bleu}} | {{Widget:Fin-cadre-Bleu}} | ||
| Ligne 44 : | Ligne 44 : | ||
<!-- Remplacer et adapter le contenu --> | <!-- Remplacer et adapter le contenu --> | ||
| − | [[Espèce chimique]] / [[Solution]] / [[Concentration molaire]] / [[Quantité de matière]] / [[Volume]] | + | [[Espèce chimique]]/ [[Solution aqueuse]] / [[Concentration molaire]] / [[Quantité de matière]] / [[Volume]] |
| Ligne 51 : | Ligne 51 : | ||
= {{Widget:Exemples-applications-utilisations-Fiche}} = | = {{Widget:Exemples-applications-utilisations-Fiche}} = | ||
| − | * | + | * C'est une méthode simple permettant de vérifier la pureté d'un composé. |
| − | * . | + | * Les responsables des eaux usées de n'importe quelle usine chimique au monde n'ont pas le droit de rejeter à la rivière les tonnes de solutions acides ou basiques issus des opérations de lavage ou les sous-produits que leurs chimistes rejettent aux égouts de l'entreprise, en le voulant ou sans le vouloir. Ils doivent les neutraliser, et c'est là qu'intervient le titrage |
| − | |||
= {{Widget:Erreurs-confusions-Fiche}} = | = {{Widget:Erreurs-confusions-Fiche}} = | ||
| − | * | + | * la courbe du dosage pH-métrique présente un obstacle à l’apprentissage de la réaction acido-basique étant donné que l’apprenant fait un rapport entre l’événement reconstruit (réaction acido-basique) et l’événement perceptible (saut de pH). |
| − | |||
= {{Widget:Questions-possibles-Fiche}} = | = {{Widget:Questions-possibles-Fiche}} = | ||
| − | * | + | * Comment peut-on identifier le point d’équivalence lors d'un dosage acido-basique? |
| − | |||
= {{Widget:Liens-enseignement-Fiche}} = | = {{Widget:Liens-enseignement-Fiche}} = | ||
| Ligne 72 : | Ligne 69 : | ||
= {{Widget:Aides-astuces-Fiche}} = | = {{Widget:Aides-astuces-Fiche}} = | ||
| − | + | Un volume donné de la solution à titrer , mesuré à l'aide d'une pipette jaugée, est versé dans un erlenmeyer ou un bécher. On remplit une burette graduée avec une solution de concentration connue de réactif titrant, que l'on ajoute progressivement à la solution à titrer. | |
= {{Widget:Difficultes-enseignement-Fiche}} = | = {{Widget:Difficultes-enseignement-Fiche}} = | ||
| − | + | Le déroulement du dosage est mal interprété par les élèves. Une représentation souvent rapportée est que l’espèce titrée et l’espèce titrante ne réagissent qu’à l’équivalence. | |
= {{Widget:Liens-internet-Fiche}} = | = {{Widget:Liens-internet-Fiche}} = | ||
| − | * | + | * http://www.lachimie.net/index.php?page=46#.WH4bgblxtdg |
| − | * | + | * http://passeport.univ-lille1.fr/site/chimie/scc1034/C10dosab/C10dosab_web.publi/web/co/Module_C10dosab_4.html |
| − | |||
= {{Widget:Bibliographie-Fiche}} = | = {{Widget:Bibliographie-Fiche}} = | ||
| Ligne 91 : | Ligne 87 : | ||
[[Category:Domaine ou Thématique ou Discipline]] | [[Category:Domaine ou Thématique ou Discipline]] | ||
[[Category: Fiches didactiques]] | [[Category: Fiches didactiques]] | ||
| + | [[Category: superviseur]] | ||
| + | [[Category: superviseur Drine]] | ||
Version actuelle datée du 11 février 2017 à 13:00
 Traduction
Traduction
Dosage acido basique (Français) / Acid-base dosage (Anglais) / جرعة الحمضي القاعدي (Arabe)
 Définition
Définition
- Domaine, Discipline, Thématique :
Catégorie: Chimie / Catégorie: Biologie / Catégorie: SVT
Définition écrite
|
Doser ou titrer une espèce chimique en solution consiste à déterminer la concentration molaire de cette espèce. Cela revient aussi à déterminer la quantité de matière de cette espèce présente dans un volume donné de cette solution.
|
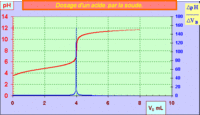
Définition graphique
 Concepts ou notions associés
Concepts ou notions associés
 Exemples, applications, utilisations
Exemples, applications, utilisations
- C'est une méthode simple permettant de vérifier la pureté d'un composé.
- Les responsables des eaux usées de n'importe quelle usine chimique au monde n'ont pas le droit de rejeter à la rivière les tonnes de solutions acides ou basiques issus des opérations de lavage ou les sous-produits que leurs chimistes rejettent aux égouts de l'entreprise, en le voulant ou sans le vouloir. Ils doivent les neutraliser, et c'est là qu'intervient le titrage
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- la courbe du dosage pH-métrique présente un obstacle à l’apprentissage de la réaction acido-basique étant donné que l’apprenant fait un rapport entre l’événement reconstruit (réaction acido-basique) et l’événement perceptible (saut de pH).
 Questions possibles
Questions possibles
- Comment peut-on identifier le point d’équivalence lors d'un dosage acido-basique?
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
- Portail Formation Gratuite
- Multisites Educatifs
- Sur DidaQuest
- Sur le Portail Didactique.info
- Sur le Portail Questions / Réponses
- Concept Sur Wikipedia
- Concept Sur Wikiwand
- Concept Sur Wikiversity
 Aides, Astuces,...
Aides, Astuces,...
Un volume donné de la solution à titrer , mesuré à l'aide d'une pipette jaugée, est versé dans un erlenmeyer ou un bécher. On remplit une burette graduée avec une solution de concentration connue de réactif titrant, que l'on ajoute progressivement à la solution à titrer.
=
 Difficultés liées à son enseignement =
Le déroulement du dosage est mal interprété par les élèves. Une représentation souvent rapportée est que l’espèce titrée et l’espèce titrante ne réagissent qu’à l’équivalence.
Difficultés liées à son enseignement =
Le déroulement du dosage est mal interprété par les élèves. Une représentation souvent rapportée est que l’espèce titrée et l’espèce titrante ne réagissent qu’à l’équivalence.
 Liens Internet
Liens Internet
- http://www.lachimie.net/index.php?page=46#.WH4bgblxtdg
- http://passeport.univ-lille1.fr/site/chimie/scc1034/C10dosab/C10dosab_web.publi/web/co/Module_C10dosab_4.html