Liaisons chimiques
 Traduction
Traduction
 Définition
Définition
Domaine, Discipline, Thématique
Définition écrite
|
|
Définition graphique
- AUTRES MEDIAS
![]() Liaisons chimiques
Liaisons chimiques
![]() chimiques Liaisons chimiques
chimiques Liaisons chimiques
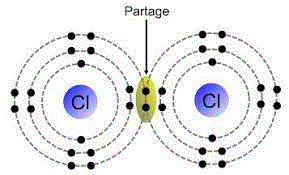
![]() Représentation graphique spatiale Liaisons chimiques
Représentation graphique spatiale Liaisons chimiques
 Concepts ou notions associés
Concepts ou notions associés
Liaison covalent / Liaison ionique / Liaison métallique / Liaison hydrogène / Polarité des Liaisons / Électronégativité / Orbitales Moléculaires / Règle de l'Octet / Énergie de Liaison / Longueur et Angle de Liaison / Résonance / Hybridation des Orbitales / Forces de Van der Waals / Liaison Sigma et Pi / Théorie de la Répulsion des Paires d'Électrons de la Couche de Valence (VSEPR) / Théorie des Orbitales Moléculaires / Liaison Coordonnée ou Dative / Stabilité des Composés / Composés Coordonnés / Règles de Lewis. /
 Exemples, applications, utilisations
Exemples, applications, utilisations
................................................................................ ................................................................................ ................................................................................
................................................................................ ................................................................................ ................................................................................ |
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- .........................................
- .........................................
![]() Confusion possible ou glissement de sens
Confusion possible ou glissement de sens
- Confusion entre Ion - Atome
- Confusion entre Polarité - Dipôle
- Confusion entre Liaison ionique - Liaison covalente polarisée
- Confusion entre Liaison covalente - Liaison métallique
- Confusion entre Hydrogène lié - Liaison hydrogène
- Confusion entre Hydrophobe - Hydrophile
- Confusion entre Energie de liaison - Energie d'ionisation
- ....................
 Questions possibles
Questions possibles
- Quelle est la différence entre une liaison covalente et une liaison ionique ?
- Comment la polarité d'une liaison chimique est-elle déterminée?
- Qu'est-ce que la règle de l'octet et comment s'applique-t-elle aux liaisons chimiques?
- Quels sont les facteurs qui influencent la force d'une liaison chimique ?
- Comment l'électronégativité affecte-t-elle les liaisons chimiques?
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
Idées ou Réflexions liées à son enseignement
L'enseignement des liaisons chimiques, un sujet complexe et fondamental en chimie, offre de nombreuses opportunités pour des approches pédagogiques innovantes et engageantes. Voici quelques idées et réflexions pour l'enseignement de ce sujet :
- Utilisation de Modèles Moléculaires : Les modèles en 3D aident les étudiants à visualiser la structure des molécules et à comprendre la spatialité des liaisons chimiques.
- Approches Basées sur des Projets : Encourager les étudiants à mener des projets de recherche sur des composés spécifiques pour explorer comment les liaisons chimiques influencent les propriétés et les usages de ces composés.
- Expériences de Laboratoire : Des expériences pratiques peuvent démontrer les effets des liaisons chimiques sur les propriétés physiques et chimiques, telles que la conductivité, la solubilité ou le point de fusion.
- Utilisation de la Technologie : Des logiciels de modélisation moléculaire ou des applications de réalité augmentée peuvent rendre l'apprentissage des liaisons chimiques plus interactif et visuel.
- Jeux et Activités Ludiques : Les jeux éducatifs et les activités de groupe peuvent rendre l'apprentissage des liaisons chimiques plus engageant et aider à mémoriser des concepts complexes.
- Discussions sur des Applications Réelles : Relier les concepts de liaisons chimiques à des applications dans la vie quotidienne, comme les médicaments, les matériaux polymères, ou l'impact environnemental.
- Enseignement Interdisciplinaire : Intégrer des aspects de physique, de biologie et même de mathématiques pour montrer comment les liaisons chimiques jouent un rôle dans divers domaines.
- Travail Collaboratif : Encourager les travaux de groupe pour favoriser l'échange d'idées et le développement de compétences en communication scientifique.
- Évaluation Formative : Utiliser des quiz et des tests réguliers pour évaluer la compréhension des étudiants et adapter les méthodes d'enseignement en conséquence.
- Approfondissement Théorique : Fournir des ressources supplémentaires pour les étudiants avancés intéressés par des aspects plus complexes des liaisons chimiques, comme la théorie orbitale moléculaire ou la chimie quantique
L'objectif est de créer un environnement d'apprentissage où les étudiants peuvent explorer, expérimenter et comprendre de manière approfondie les concepts de liaisons chimiques, tout en développant des compétences en résolution de problèmes et en pensée critique.
Aides et astuces
Education: Autres liens, sites ou portails
 Bibliographie
Bibliographie
Pour citer cette page: (chimiques)
ABROUGUI, M & al, 2023. Liaisons chimiques. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Liaisons_chimiques>, consulté le 24, novembre, 2024
- ..................
- ..................
- ..................
- ..................
- Sponsors Education
- Chimie (Concepts)
- Physique (Concepts)
- Sciences de Matériaux (Concepts)
- Didactique (Concepts)
- Epistémologie (Concepts)
- Liaison covalent
- Liaison ionique
- Liaison métallique
- Liaison hydrogène
- Polarité des Liaisons
- Électronégativité
- Orbitales Moléculaires
- Règle de l'Octet
- Énergie de Liaison
- Longueur et Angle de Liaison
- Résonance
- Hybridation des Orbitales
- Forces de Van der Waals
- Liaison Sigma et Pi
- Théorie de la Répulsion des Paires d'Électrons de la Couche de Valence (VSEPR)
- Théorie des Orbitales Moléculaires
- Liaison Coordonnée ou Dative
- Stabilité des Composés
- Composés Coordonnés
- Règles de Lewis.
- Concepts
- Liaisons chimiques
- Liaisons chimiques (Concepts)
- Fiche conceptuelle didactique