Tension - Courant
 Conception : Clarification - Explicitation
Conception : Clarification - Explicitation
- L'absorbance (A) et la transmittance (T) sont deux concepts fondamentaux en spectroscopie qui sont liés mathématiquement. Ces concepts sont généralement utilisés pour quantifier l'interaction d'un échantillon avec la lumière. Voici les conceptions canoniques de l'absorbance et de la transmittance :
Absorbance (A) :
Définition : L'absorbance est une mesure de la capacité d'un matériau à absorber la lumière à une longueur d'onde spécifique. Caractéristiques : L'absorbance est une grandeur sans dimension, et elle est directement proportionnelle à l'épaisseur de l'échantillon traversé par la lumière et à la concentration de la substance absorbante.
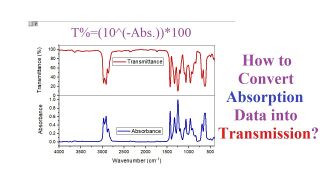
Transmittance (T) : Définition : La transmittance mesure la fraction de lumière qui traverse un échantillon par rapport à la lumière incidente. Caractéristiques : La transmittance est généralement exprimée en pourcentage (0% à 100%) et est inversement proportionnelle à l'absorbance. En spectroscopie, ces deux concepts sont souvent utilisés pour quantifier la quantité d'une substance absorbante dans un échantillon. Une forte absorbance est associée à une faible transmittance et vice versa. La relation logarithmique entre l'absorbance et la transmittance est particulièrement utile car elle permet de rendre compte des variations sur une échelle plus facilement interprétable. Ces conceptions canoniques sont largement utilisées dans divers domaines scientifiques, notamment la spectroscopie UV-Visible, la spectroscopie infrarouge, et d'autres techniques spectroscopiques.
![]() Conceptions erronées et origines possibles
Conceptions erronées et origines possibles
- Confusion entre l'absorbance et la concentration : Une conception erronée est de penser que l'absorbance est directement proportionnelle à la concentration de l'échantillon. En réalité, l'absorbance dépend de divers facteurs, notamment la concentration, l'épaisseur de l'échantillon, et le coefficient d'absorption molaire.
Interprétation incorrecte de l'unité de l'absorbance : Certains peuvent mal interpréter l'unité de l'absorbance, pensant qu'elle est en pourcentage ou en unité de longueur. En fait, l'absorbance est sans dimension et exprimée en log base 10 de l'inverse de la transmittance.
Penser que la transmittance est une mesure directe de la concentration : Une conception erronée est de considérer la transmittance comme une mesure directe de la concentration de la substance absorbante. Bien que la transmittance diminue avec l'augmentation de la concentration, elle dépend également de l'épaisseur de l'échantillon.
Ignorer les variations de longueur d'onde : Une erreur courante est de ne pas tenir compte des variations de longueur d'onde dans l'absorbance. La relation entre l'absorbance et la concentration dépend de la longueur d'onde spécifique de la lumière utilisée.
Penser que l'absorbance peut dépasser zéro : Certains peuvent mal interpréter les valeurs d'absorbance, pensant qu'elles peuvent être positives. En réalité, l'absorbance est définie comme le logarithme négatif de la transmittance, ce qui signifie qu'elle est toujours négative ou nulle.
Il est crucial, lors de l'enseignement de la spectroscopie, de clarifier ces concepts et de souligner les conditions et les facteurs qui influent sur l'absorbance et la transmittance. Des démonstrations pratiques et des exemples concrets peuvent aider à prévenir ces conceptions erronées.
![]() Conceptions: Origines possibles
Conceptions: Origines possibles
- Analogie avec la lumière visible : Les personnes peuvent être tentées de faire des analogies simplifiées avec leur expérience quotidienne de la lumière visible. Par exemple, penser que l'absorbance est directement comparable à l'opacité d'un matériau dans la lumière visible, ce qui peut conduire à une mauvaise interprétation des concepts spectroscopiques.
Interprétation superficielle des formules : Les formules mathématiques liant l'absorbance et la transmittance peuvent être mal interprétées, particulièrement si l'enseignement ne met pas suffisamment l'accent sur leur signification physique. Par exemple, ne pas comprendre que l'absorbance est le logarithme négatif de la transmittance
Simplification excessive des relations causales : Certains étudiants peuvent avoir une compréhension trop simplifiée des relations causales entre la concentration d'une substance absorbante, l'épaisseur de l'échantillon et l'absorbance. Ils pourraient penser que l'absorbance dépend uniquement de la concentration, sans tenir compte d'autres facteurs.
Lack of Hands-On Experience: A lack of hands-on experience with spectrophotometric techniques can contribute to misconceptions. Without practical exposure to manipulating instruments, preparing samples, and interpreting spectra, students may struggle to connect theoretical concepts with real-world applications.
Confusion avec d'autres mesures de transmission de la lumière : La confusion peut également découler de la similarité des termes tels que "transmission" dans le contexte de la transmittance et "transparent" dans le contexte de la lumière visible, créant des associations inappropriées.
Réduction des concepts complexes : La spectroscopie peut être un domaine complexe, et certains enseignants ou apprenants peuvent être tentés de simplifier excessivement les concepts pour faciliter la compréhension. Cependant, cela peut entraîner des simplifications excessives et des erreurs conceptuelles.
Pour éviter ces conceptions erronées, il est essentiel d'adopter une approche pédagogique qui met l'accent sur la compréhension profonde des concepts, en utilisant des exemples concrets et des applications pratiques. Les démonstrations en laboratoire et les exercices interactifs peuvent également contribuer à renforcer la compréhension correcte de l'absorbance et de la transmittance.
 Conceptions liées - Typologie
Conceptions liées - Typologie
 Concepts ou notions associés
Concepts ou notions associés
| Références
| |||
|---|---|---|---|
|
Sur le Portail Questions / Réponses |
Sur Portail de Formation Gratuite |
Sur des sites de Formation |
Sur DidaQuest |
| Tension - Courant sur : Wikipedia / Wikiwand / Universalis / Larousse encyclopédie / Khan Académie | |||
| Sur Wikiwand :
Loi de Beer-Lambert / Coefficient d'absorption molaire / Transmittance / Longueur d'onde / Pic d'absorption | |||
| Sur Wikipédia :
Loi de Beer-Lambert / Coefficient d'absorption molaire / Transmittance / Longueur d'onde / Pic d'absorption | |||
| Sur Wikiversity :
Loi de Beer-Lambert / Coefficient d'absorption molaire / Transmittance / Longueur d'onde / Pic d'absorption | |||
| Sur Universalis :
Loi de Beer-Lambert / Coefficient d'absorption molaire / Transmittance / Longueur d'onde / Pic d'absorption | |||
| Sur Khan Académie :
Loi de Beer-Lambert / Coefficient d'absorption molaire / Transmittance / Longueur d'onde / Pic d'absorption | |||
 Éléments graphique
Éléments graphique
 Stratégie de changement conceptuel
Stratégie de changement conceptuel
- Diagnostic des Conceptions Erronées :
Identifiez les conceptions erronées spécifiques que les apprenants ont sur l'absorbance et la transmittance. Cela peut être fait par le biais de discussions en classe, de questions ouvertes, ou même de quiz diagnostiques.
- Clarification des Concepts Fondamentaux :
Revenez sur les concepts fondamentaux, en mettant l'accent sur des définitions claires et précises de l'absorbance et de la transmittance. Utilisez des exemples concrets pour illustrer ces concepts.
- Utilisation d'Analogies Appropriées :
Utilisez des analogies simples mais précises pour aider à expliquer les relations entre l'absorbance, la transmittance, et d'autres concepts associés. Par exemple, une analogie avec le filtre solaire pour illustrer la transmittance.
- Démonstrations Pratiques :
Intégrez des démonstrations pratiques en laboratoire ou des simulations virtuelles qui permettent aux apprenants de visualiser les changements dans l'absorbance et la transmittance en fonction de différentes conditions expérimentales.
 Questions possibles
Questions possibles
 Bibliographie
Bibliographie
Pour citer cette page: (- Courant)
ABROUGUI, M & al, 2024. Tension - Courant. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Tension_-_Courant>, consulté le 1, juin, 2025
- Harris, D. C. (2010). Quantitative Chemical Analysis. W. H. Freeman.
- Banwell, C. N., & McCash, E. M. (1994). Fundamentals of Molecular Spectroscopy. McGraw-Hill.
- Skoog, D. A., Holler, F. J., & Crouch, S. R. (2007). Principles of Instrumental Analysis. Cengage Learning.
- Silverstein, R. M., Webster, F. X., & Kiemle, D. J. (2004). Spectrometric Identification of Organic Compounds. Wiley.
- Sponsors Question
- Dépendance de la concentration - Conceptions
- Coefficient d'absorption molaire - Conceptions
- Épaisseur de l'échantillon - Conceptions
- Complémentarité avec l'absorbance - Conceptions
- Effet de matrice - Conceptions
- Loi de Beer-Lambert - Conceptions
- Spectrophotométrie UV-Visible - Conceptions
- Spectroscopie infrarouge - Conceptions
- Baselines et bruit - Conceptions
- Conceptions
- Transmittance - Conceptions
- Longueur d'onde - Conceptions
- Pic d'absorption - Conceptions
- Étalonnage - Conceptions
- Fiches Conceptions
- Fiche Conceptions