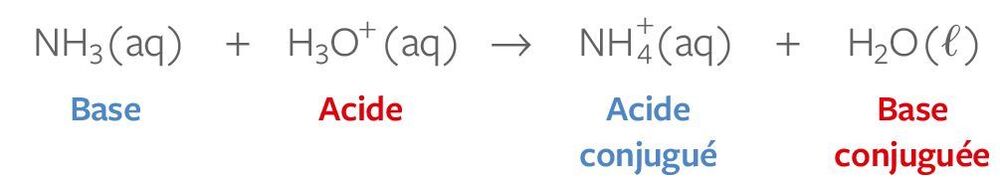Acides et Bases
De Didaquest
Révision datée du 6 février 2023 à 22:52 par Fathiomar (discussion | contributions) (→{{Widget:Questions-possibles-Fiche}})
 Traduction
Traduction
 Définition
Définition
Domaine, Discipline, Thématique
Définition écrite
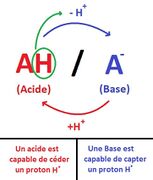
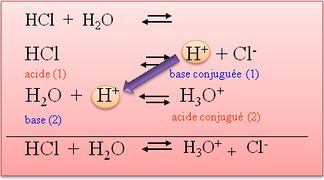
- Un acide est une substance chimique qui a une teneur élevée en ions hydronium (H3O+) en solution. Les acides peuvent réagir avec les bases pour former des sels et de l'eau. Les acides sont souvent décrits comme ayant un goût aigre et une réaction avec des métaux pour produire des gaz comme le dioxyde de carbone ou de l'hydrogène.
- Une base est une substance chimique différente d'un acide. Les bases ont une teneur élevée en ions hydroxyle (OH-) en solution et peuvent réagir avec les acides pour former des sels et de l'eau. Les bases sont souvent décrites comme ayant un goût alcalin et une réaction avec les acides pour produire une solution tamponée, ce qui signifie que le pH de la solution reste relativement stable.
|
Définition graphique
 Concepts ou notions associés
Concepts ou notions associés
 Exemples, applications, utilisations
Exemples, applications, utilisations
|
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- Le ph d'un acide est élevé implique que l'acide est fort.
- l'acide est plus dangereux que la base.
![]() Confusion possible ou glissement de sens
Confusion possible ou glissement de sens
- Confusion entre ph de la base - ph de l'acide
- Confusion entre l'ionisation de la base - l'ionisation de l'acide
- Pour préparer une solution diluée d'un acide ou d'une base, il faut impérativement verser de l'acide ou de la base dans l'eau et ne pas l'inverse.
 Questions possibles
Questions possibles
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
Idées ou Réflexions liées à son enseignement
Aides et astuces
Education: Autres liens, sites ou portails
 Bibliographie
Bibliographie
Pour citer cette page: (et Bases)
ABROUGUI, M & al, 2023. Acides et Bases. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Acides_et_Bases>, consulté le 12, mai, 2025
- ..................
- ..................
- ..................
- ..................
Catégories :
- Sponsors Education
- Chimie organique (Concepts)
- Chimie minérale (Concepts)
- Chimie pharmacetique (Concepts)
- Industrie Alimentaire (Concepts)
- Détergeant (Concepts)
- Cosmétique (Concepts)
- Anatomie (Concepts)
- Propriétés chimiques
- Constante d'acidité (pKa)
- Réaction d'acid-base
- Equilibre acide-base
- Equation de réaction d'acide-base
- Neutralisation
- PH
- Constante de basicité (Pkb)
- Dosage acido-basique
- Dosage volumétrique
- Concepts
- Acides et Bases
- Acides et Bases (Concepts)
- Fiche conceptuelle didactique