Différences entre versions de « Base faible et base forte »
De Didaquest
Aller à la navigationAller à la recherche| (8 versions intermédiaires par le même utilisateur non affichées) | |||
| Ligne 61 : | Ligne 61 : | ||
|Concept-lié-1=la force de 2 bases faibles B1 et B2 de même concentration | |Concept-lié-1=la force de 2 bases faibles B1 et B2 de même concentration | ||
|Concept-lié-2=le coefficient le dissociation a | |Concept-lié-2=le coefficient le dissociation a | ||
| − | |Concept-lié-3=la constante | + | |Concept-lié-3=la constante pKb |
|Concept-lié-4=l'échelle du pH | |Concept-lié-4=l'échelle du pH | ||
|Concept-lié-5=la dilution d'une soluion basique | |Concept-lié-5=la dilution d'une soluion basique | ||
| Ligne 80 : | Ligne 80 : | ||
<!-- Remplacez, Adaptez, Ajoutez ou Supprimez les images et lignes non utilisées--> | <!-- Remplacez, Adaptez, Ajoutez ou Supprimez les images et lignes non utilisées--> | ||
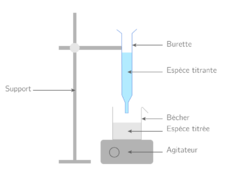
| − | Image: | + | Image:montage_titrage acido-basique.png|montage_titrage acido-basique |
| − | |||
| − | |||
| − | |||
</gallery><!-- ************** Fin modification images***************************--> | </gallery><!-- ************** Fin modification images***************************--> | ||
<!-- ************************* Début modification Vidéo ******************************************************************--> | <!-- ************************* Début modification Vidéo ******************************************************************--> | ||
| Ligne 93 : | Ligne 90 : | ||
<!-- ****************** Commercez les modifications pour les Vidéos *******************************************************--> | <!-- ****************** Commercez les modifications pour les Vidéos *******************************************************--> | ||
| − | <youtube width="220" height="220"> | + | <youtube width="220" height="220">https://www.youtube.com/watch?v=uj5awfuSiJI</youtube> |
| − | <youtube width="220" height="220"> | + | <youtube width="220" height="220">https://www.youtube.com/watch?v=NcDI1HOuIto</youtube> |
| − | + | ||
}}<!-- ************************* Fin modifications pour les Médias *******************************************************--> | }}<!-- ************************* Fin modifications pour les Médias *******************************************************--> | ||
| − | |||
= {{Widget:Stratégie de changement conceptuelle : Solutions possibles}} = | = {{Widget:Stratégie de changement conceptuelle : Solutions possibles}} = | ||
| Ligne 125 : | Ligne 121 : | ||
<!-- ************ Commercez les modifications *********************--> | <!-- ************ Commercez les modifications *********************--> | ||
| − | * [[ | + | * [[Comment déterminer la concentration inconnue d'une solution basique ?]] |
| − | + | ||
| − | |||
}}<!-- ******** Fin Fiche Didactique Questions ******************* --> | }}<!-- ******** Fin Fiche Didactique Questions ******************* --> | ||
| Ligne 139 : | Ligne 134 : | ||
<!-- ****************** Commercez les modifications *********************--> | <!-- ****************** Commercez les modifications *********************--> | ||
| − | * .. | + | * acides bases - exercice - Terminale ST2S - MOOC#1 [[https://www.youtube.com/watch?v=tF40PBrSpN4]] |
| − | |||
| − | |||
| − | |||
}}<!-- ************* Fin Fiche Didactique Bibliographie *************** --> | }}<!-- ************* Fin Fiche Didactique Bibliographie *************** --> | ||
{{Widget:Fiche-Conceptions-Bas}} | {{Widget:Fiche-Conceptions-Bas}} | ||
Version actuelle datée du 4 janvier 2020 à 08:19
 Conception : Clarification - Explicitation
Conception : Clarification - Explicitation
- La base la plus forte possède la valeur du pH la plus grande
Pour une base forte : Si Cb représente la concentration de la base alors [OH-]= Cb donc : pH = pKe + log Cb Pour une base faible : Si Cb représente la concentration de la base alors [OH-] <Cb donc pH < pKe + log Cb
De plus :
Pour une base forte : Le coefficient le dissociation a ; a = [OH-]/Cb = 1 Pour une base faible : Le coefficient le dissociation a ; a = [OH-]/Cb < 1 d'ou a augmente quand Cb diminue On peut conclure :
Pour une base forte : La réaction avec l'eau est totale: B + H2O →BH+ + OH- Pour une base faible : La réaction avec l'eau n'est pas totale: B + H2O<=>BH+ + OH-
![]() Conceptions erronées et origines possibles
Conceptions erronées et origines possibles
- la base la plus forte possède la valeur du pH la plus faible
![]() Conceptions: Origines possibles
Conceptions: Origines possibles
- Si l'individu ne connait pas l'échelle du pH alors ne sais plus le sens de basicité croissante donc ne peut pas faire une comparaison juste de deux acides
 Conceptions liées - Typologie
Conceptions liées - Typologie
 Concepts ou notions associés
Concepts ou notions associés
 Éléments graphique
Éléments graphique
 Stratégie de changement conceptuel
Stratégie de changement conceptuel
 Questions possibles
Questions possibles
 Bibliographie
Bibliographie
Pour citer cette page: (faible et base forte)
ABROUGUI, M & al, 2020. Base faible et base forte. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Base_faible_et_base_forte>, consulté le 24, novembre, 2024
- acides bases - exercice - Terminale ST2S - MOOC#1 [[1]]
Catégories :
- Sponsors Question
- Erreur liée aux opérations intellectuelles impliquées - Conceptions
- Erreur causée par la complexité du contenu - Conceptions
- Erreur portant sur les démarches adoptées - Conceptions
- Conceptions
- La force de 2 bases faibles B1 et B2 de même concentration - Conceptions
- Le coefficient le dissociation a - Conceptions
- La constante pKb - Conceptions
- L'échelle du pH - Conceptions
- La dilution d'une soluion basique - Conceptions
- La concentration d'une base - Conceptions
- Fiches Conceptions
- Fiche Conceptions