Différences entre versions de « Notion de pH »
De Didaquest
Aller à la navigationAller à la recherche| Ligne 89 : | Ligne 89 : | ||
<youtube width="220" height="220">=dldIraKTrHY</youtube> | <youtube width="220" height="220">=dldIraKTrHY</youtube> | ||
| − | <youtube width="220" height="220"> | + | <youtube width="220" height="220">=BxEXjEGjHRQ</youtube> |
<youtube width="220" height="220">k0O8-0kPQmM</youtube> | <youtube width="220" height="220">k0O8-0kPQmM</youtube> | ||
Version du 7 décembre 2019 à 09:33
 Traduction
Traduction
 Définition
Définition
Domaine, Discipline, Thématique
Définition écrite
- Le pH permet de caractériser l’acidité ou la basicité d’une solution. Il est défini par la relation : [H3O+] = 10-pH.
|
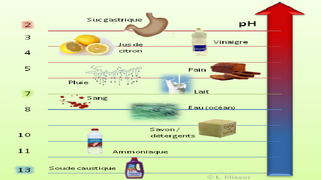
Définition graphique
 Concepts ou notions associés
Concepts ou notions associés
 Exemples, applications, utilisations
Exemples, applications, utilisations
|
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- Confusion entre acide et base
- Confusion entre acide faible et acide fort
- Confusion entre base faible et acide forte
- Erreur fréquente: ....................
 Questions possibles
Questions possibles
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
Idées ou Réflexions liées à son enseignement
Aides et astuces
Education: Autres liens, sites ou portails
 Bibliographie
Bibliographie
Pour citer cette page: (de pH)
ABROUGUI, M & al, 2019. Notion de pH. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Notion_de_pH>, consulté le 21, novembre, 2024
- ..................
- ..................
- ..................
- ..................
Catégories :
- Sponsors Education
- Chimie (Concepts)
- Acides (Concepts)
- Bases (Concepts)
- Milieu neutre (Concepts)
- Fruits (Concepts)
- Légumes (Concepts)
- Détergeant (Concepts)
- Chimie
- Acides
- Bases
- Milieu neutre
- Industrie alimentaire
- Industrie agroalimentaire
- Industrie pharmaceutique
- Industrie cosmétique
- Industrie de fabrication de détergents et de produits de nettoyage
- Concepts
- Notion de pH
- Notion de pH (Concepts)
- Fiche conceptuelle didactique