Réaction acido basique
 Traduction
Traduction
Réaction acido basique (Français)
/ Acid–base reaction (Anglais)
/ التفاعل الحمضي-القاعدي (Arabe)
 Définition
Définition
Domaine, Discipline, Thématique
Définition écrite
- ......................................................................
....................................................................... ....................................................................... .......................................................................
- ......................................................................
.......................................................................
.......................................................................
....................................................................... ....................................................................... .......................................................................
....................................................................... ....................................................................... |
Définition graphique
 Concepts ou notions associés
Concepts ou notions associés
 Exemples, applications, utilisations
Exemples, applications, utilisations
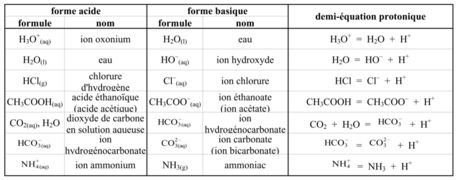
Demi-équation du couple A1/B1 : CH3COOH(aq) = CH3COO−(aq) + H+ Demi-équation du couple A2/B2 (inversée) : HO−(aq) + H+ = H2O(l) Équation de la réaction acido-basique : CH3COOH(aq) + HO−(aq) → CH3COO−(aq) + H2O(l)
................................................................................ ................................................................................ ................................................................................ |
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- Confusion entre acide et base
- Confusion entre acide fort et acide faibe
- Confusion entre équation bilan et base demi-équation
- Erreur fréquente: ....................
 Questions possibles
Questions possibles
- [[ On prépare une solution en mettant une masse m=0,32g de chlorure d'ammonium dans un volume V=100mL d'eau sans variation de volume. Le pH de la solution obtenue est pH=5,2.
1. Donner l'équation de dissolution du chlorure d'ammonium.
2. Montrer que l'ion ammonium est un acide faible.
3. Donner l'équation de la réaction entre l'ion ammonium et l'eau. ]]
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
Idées ou Réflexions liées à son enseignement
Aides et astuces
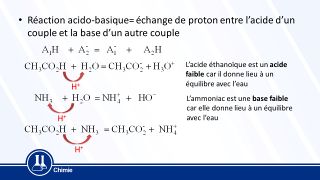
- Le couple Acide/Base est de la forme :
AH / A−
La demi-équation Acide/Base correspondante est :
AH <=> A− + H+
- Une espèce à la fois base conjuguée d'un couple et acide conjugué d'un autre est appelée ampholyte ou amphotère : elle peut réagir comme une base ou comme un acide.
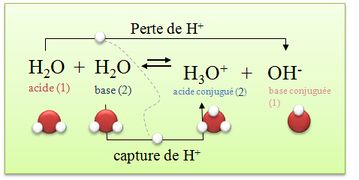
exemple : * H3O+/ H2O(l) : dans ce couple l’eau est une base H3O+ = H2O(l) + H+
*H2O / HO-(aq) : dans ce couple l’eau est un acide H2O = HO-(aq) + H+
=> L'eau peut être un acide ou une base. On dit que l’eau est un ampholyte ou une espèce amphotère.
- .................
Education: Autres liens, sites ou portails
 Bibliographie
Bibliographie
Pour citer cette page: (acido basique)
ABROUGUI, M & al, 2019. Réaction acido basique. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/R%C3%A9action_acido_basique>, consulté le 24, novembre, 2024
- ..................
- ..................
- ..................
- ..................