Différences entre versions de « Solution en chimie »
De Didaquest
Aller à la navigationAller à la recherche| Ligne 49 : | Ligne 49 : | ||
<!-- *************** Commercez les modifications *******************--> | <!-- *************** Commercez les modifications *******************--> | ||
| − | *Mélange liquide homogène d'une ou plusieurs substance(s) solide(s), liquide(s) ou gazeuse(s), le soluté, et d'un liquide, le solvant. | + | * Mélange liquide homogène d'une ou plusieurs substance(s) solide(s), liquide(s) ou gazeuse(s), le soluté, et d'un liquide, le solvant. |
| − | *On appelle solution un mélange constitué d'un solvant, l'espèce majoritaire, et d'un ou plusieurs solutés, les espèces minoritaires placées dans le solvant. | + | |
| − | *Le soluté peut être à l’état solide, liquide ou gazeux et il se dissout dans le solvant. La solution obtenue (mélange homogène du soluté et du solvant) peut être solide ou liquide (en pratique on ne parle pas de solution pour un mélange homogène de gaz) | + | * Qu’est-ce qu’un mélange ? |
| + | C'est l'opération qui consiste à réunir plusieurs composants, à les mêler. Un ensemble ainsi constitué peut être: | ||
| + | :- hétérogène : on voit des substances en suspension ou en dépôt (ex. : eau + farine), ou | ||
| + | : - homogène : on ne distingue plus les différents constituants. | ||
| + | :: Ex.: mélange homogène solide (farine + plâtre), | ||
| + | :: Ex.: mélange homogène liquide (eau + alcool), | ||
| + | :: Ex.: mélange homogène gazeux (air). | ||
| + | |||
| + | * On appelle solution un mélange constitué d'un solvant, l'espèce majoritaire, et d'un ou plusieurs solutés, les espèces minoritaires placées dans le solvant. | ||
| + | * Le soluté peut être à l’état solide, liquide ou gazeux et il se dissout dans le solvant. La solution obtenue (mélange homogène du soluté et du solvant) peut être solide ou liquide (en pratique on ne parle pas de solution pour un mélange homogène de gaz) | ||
| + | |||
| + | |||
<!-- ******** Fin Définition Générale ***************************** --> | <!-- ******** Fin Définition Générale ***************************** --> | ||
<!-- ************* Début Définition Approfondissement ************* --> | <!-- ************* Début Définition Approfondissement ************* --> | ||
| Ligne 57 : | Ligne 68 : | ||
|Typologie= <!------------------------------------ Ne pas Modifier --> | |Typologie= <!------------------------------------ Ne pas Modifier --> | ||
<!-- ****************** Commercez les modifications ****************--> | <!-- ****************** Commercez les modifications ****************--> | ||
| + | * Une solution, c'est avant tout un mélange. Plus précisément, un mélange homogène liquide (eau et sel ou eau et sucre) ou solide (alliage). Dans ce mélange, l'un des composants joue un rôle différent des autres. Si on prend le cas d'une solution d'eau sucrée, l'eau est ce que l'on appelle le [[solvant]] (en plus grande quantité) et le sucre le [[soluté]]. Dans ces mélanges homogènes, on ne peut distinguer le [[soluté]]. | ||
| + | |||
| + | * Toute solution dont l'eau constitue le solvant est qualifiée de solution aqueuse. | ||
| + | L'[[eau]] est un excellent [[solvant]], un des meilleurs solvants naturels. Le [[soluté]] peut être liquide (eau et vin !), solide (eau salée) ou gazeux (eau gazeuse). L'opération ainsi réalisée s'appelle une [[dissolution]]. | ||
| + | * Solution: - mélange liquide ou solide | ||
| + | :- mélange homogène (= dont on ne peut distinguer les différents constituants) - constituée d'un solvant (en plus grande quantité) et d'un ou plusieurs solutés sous forme solide, liquide ou gazeuse | ||
| + | :- on ne peut séparer le soluté du solvant ni par filtration, ni par décantation | ||
| + | |||
| + | |||
| + | |||
* [[Solution colloïdale]]. Solution dans laquelle le solvant est un liquide et le soluté un solide disséminé de manière homogène sous forme de très fines particules, la préparation étant soit un sol, soit un gel. Synon. suspension; anton. solution vraie.Les solutions colloïdales sont formées d'une suspension de fines particules (granules ou micelles) (Gasnier,Dépôts métall., 1927, p. 185). | * [[Solution colloïdale]]. Solution dans laquelle le solvant est un liquide et le soluté un solide disséminé de manière homogène sous forme de très fines particules, la préparation étant soit un sol, soit un gel. Synon. suspension; anton. solution vraie.Les solutions colloïdales sont formées d'une suspension de fines particules (granules ou micelles) (Gasnier,Dépôts métall., 1927, p. 185). | ||
* [[Solution vraie]]. Solution dans laquelle le ou les soluté(s) sont à l'état de division moléculaire dans le solvant. Synon. cour. solution; anton. solution colloïdale.Ces produits sont transportés dans l'air à l'état solide, et, dans l'eau, à l'état de suspensions, de solutions colloïdales ou de solutions vraies (Brajnikov,Pétrogr. et rayons X, 1936, p. 9). | * [[Solution vraie]]. Solution dans laquelle le ou les soluté(s) sont à l'état de division moléculaire dans le solvant. Synon. cour. solution; anton. solution colloïdale.Ces produits sont transportés dans l'air à l'état solide, et, dans l'eau, à l'état de suspensions, de solutions colloïdales ou de solutions vraies (Brajnikov,Pétrogr. et rayons X, 1936, p. 9). | ||
| Ligne 62 : | Ligne 83 : | ||
** [[Solution solide de substitution]]. Système où les atomes dissous se substituent aux atomes solvants, le système cristallin du produit de base étant conservé. L'alliage est stable aux températures élevées sous la forme d'une solution solide de substitution désordonnée; aux basses températures, il se trouve sous une forme ordonnée qui peut être considérée comme un composé défini (Encyclop. univ.t. 11968, p. 776). | ** [[Solution solide de substitution]]. Système où les atomes dissous se substituent aux atomes solvants, le système cristallin du produit de base étant conservé. L'alliage est stable aux températures élevées sous la forme d'une solution solide de substitution désordonnée; aux basses températures, il se trouve sous une forme ordonnée qui peut être considérée comme un composé défini (Encyclop. univ.t. 11968, p. 776). | ||
** [[Solution solide d'insertion]], d'addition. Système où les atomes dissous occupent les interstices du réseau cristallin du produit de base. Dans le cas des solutions solides d'addition, les atomes subtitués occupent des positions interstitielles dans le réseau de l'hôte. Ces solutions solides sont fréquentes dans les phyllosilicates et tectosilicates: minéraux des argiles et zéolites (Encyclop. univ.t. 111971, p. 49). | ** [[Solution solide d'insertion]], d'addition. Système où les atomes dissous occupent les interstices du réseau cristallin du produit de base. Dans le cas des solutions solides d'addition, les atomes subtitués occupent des positions interstitielles dans le réseau de l'hôte. Ces solutions solides sont fréquentes dans les phyllosilicates et tectosilicates: minéraux des argiles et zéolites (Encyclop. univ.t. 111971, p. 49). | ||
| − | + | ||
| + | : '''Solutions de titre ou de dosage particulier''' | ||
* [[Solution saturée]]. Solution contenant autant de soluté que le solvant peut en dissoudre pour arriver à la limite de saturation. Le polissage terminé, on attaque la surface traitée par des solutions acides (...). On emploie également l'acide picrique en solution saturée dans cet alcool | * [[Solution saturée]]. Solution contenant autant de soluté que le solvant peut en dissoudre pour arriver à la limite de saturation. Le polissage terminé, on attaque la surface traitée par des solutions acides (...). On emploie également l'acide picrique en solution saturée dans cet alcool | ||
* [[Solution normale]]. Solution contenant une valence-gramme (poids atomique divisé par la valence du corps) de substance dissoute par litre. Dans la solution de ce résidu on dosait le chlore par comparaison avec une solution normale | * [[Solution normale]]. Solution contenant une valence-gramme (poids atomique divisé par la valence du corps) de substance dissoute par litre. Dans la solution de ce résidu on dosait le chlore par comparaison avec une solution normale | ||
Version du 9 février 2020 à 10:07
 Traduction
Traduction
 Définition
Définition
Domaine, Discipline, Thématique
Définition écrite
- Mélange liquide homogène d'une ou plusieurs substance(s) solide(s), liquide(s) ou gazeuse(s), le soluté, et d'un liquide, le solvant.
- Qu’est-ce qu’un mélange ?
C'est l'opération qui consiste à réunir plusieurs composants, à les mêler. Un ensemble ainsi constitué peut être:
- - hétérogène : on voit des substances en suspension ou en dépôt (ex. : eau + farine), ou
- - homogène : on ne distingue plus les différents constituants.
- Ex.: mélange homogène solide (farine + plâtre),
- Ex.: mélange homogène liquide (eau + alcool),
- Ex.: mélange homogène gazeux (air).
- On appelle solution un mélange constitué d'un solvant, l'espèce majoritaire, et d'un ou plusieurs solutés, les espèces minoritaires placées dans le solvant.
- Le soluté peut être à l’état solide, liquide ou gazeux et il se dissout dans le solvant. La solution obtenue (mélange homogène du soluté et du solvant) peut être solide ou liquide (en pratique on ne parle pas de solution pour un mélange homogène de gaz)
L'eau est un excellent solvant, un des meilleurs solvants naturels. Le soluté peut être liquide (eau et vin !), solide (eau salée) ou gazeux (eau gazeuse). L'opération ainsi réalisée s'appelle une dissolution.
|
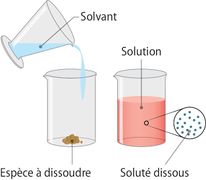
Définition graphique
 Concepts ou notions associés
Concepts ou notions associés
 Exemples, applications, utilisations
Exemples, applications, utilisations
|
Un verre de grenadine : Soluté = sirop (liquide) et Solvant = eau (liquide) Un verre de soda : Soluté = dioxyde de carbone CO2 (gaz) et Solvant = eau (liquide) Un verre d’eau sucrée (ou salée) : Soluté = sucre en poudre (solide) et Solvant = eau (liquide) |
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- Confusion entre solution et réaction chimique
- Confusion entre solution et mélange
- Confusion entre solution et dissolution
- Erreur fréquente:Si l'un des constituants du mélange est en gros excès par rapport à tous les autres composants de ce mélange, alors il s'agit d'une solution.Or,Attention, pour que l'on puisse parler de solution, il faut que le liquide soit homogène c'est à dire que le liquide doit être constitué d'une seule phase.
- Erreur fréquente:une solution est toujours à l'état liquide or, Le soluté peut être à l’état solide, liquide ou gazeux et il se dissout dans le solvant. La solution obtenue (mélange homogène du soluté et du solvant) peut être solide ou liquide (en pratique on ne parle pas de solution pour un mélange homogène de gaz).Solution solide. Mélange de plusieurs corps extrêmement visqueux intervenant dans la formation de certains alliages et de certains composés minéraux qui, après solidification, offre une structure parfaitement homogène.
 Questions possibles
Questions possibles
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
Idées ou Réflexions liées à son enseignement
Aides et astuces
Education: Autres liens, sites ou portails
 Bibliographie
Bibliographie
Pour citer cette page: (en chimie)
ABROUGUI, M & al, 2020. Solution en chimie. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Solution_en_chimie>, consulté le 23, décembre, 2024
- ..................
- ..................
- ..................
- ..................