Solution en chimie
De Didaquest
Aller à la navigationAller à la recherche
 Traduction
Traduction
 Définition
Définition
Domaine, Discipline, Thématique
Définition écrite
- Mélange liquide homogène d'une ou plusieurs substance(s) solide(s), liquide(s) ou gazeuse(s), le soluté, et d'un liquide, le solvant.
- Qu’est-ce qu’un mélange ?
C'est l'opération qui consiste à réunir plusieurs composants, à les mêler. Un ensemble ainsi constitué peut être:
- - hétérogène : on voit des substances en suspension ou en dépôt (ex. : eau + farine), ou
- - homogène : on ne distingue plus les différents constituants.
- Ex.: mélange homogène solide (farine + plâtre),
- Ex.: mélange homogène liquide (eau + alcool),
- Ex.: mélange homogène gazeux (air).
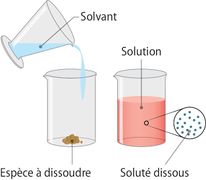
- On appelle solution un mélange constitué d'un solvant, l'espèce majoritaire, et d'un ou plusieurs solutés, les espèces minoritaires placées dans le solvant.
- Le soluté peut être à l’état solide, liquide ou gazeux et il se dissout dans le solvant. La solution obtenue (mélange homogène du soluté et du solvant) peut être solide ou liquide (en pratique on ne parle pas de solution pour un mélange homogène de gaz)
L'eau est un excellent solvant, un des meilleurs solvants naturels. Le soluté peut être liquide (eau et vin !), solide (eau salée) ou gazeux (eau gazeuse). L'opération ainsi réalisée s'appelle une dissolution.
|
Définition graphique
 Concepts ou notions associés
Concepts ou notions associés
 Exemples, applications, utilisations
Exemples, applications, utilisations
|
 Erreurs ou confusions éventuelles
Erreurs ou confusions éventuelles
- Confusion entre Solution - Mélange hétérogène
- Confusion entre Solution - Solution aqueuse
- Confusion entre Solution - Réaction chimique
- Confusion entre Solution - Mélange
- Confusion entre Solution - Dissolution
- Confusion entre Eau limpide - Eau pure - Eau potable
- Erreur fréquente: Une solution est toujours à l'état liquide or, Le soluté peut être à l’état solide, liquide ou gazeux et il se dissout dans le solvant. La solution obtenue (mélange homogène du soluté et du solvant) peut être solide ou liquide (en pratique on ne parle pas de solution pour un mélange homogène de gaz).Solution solide. Mélange de plusieurs corps extrêmement visqueux intervenant dans la formation de certains alliages et de certains composés minéraux qui, après solidification, offre une structure parfaitement homogène.
 Questions possibles
Questions possibles
 Liaisons enseignements et programmes
Liaisons enseignements et programmes
Idées ou Réflexions liées à son enseignement
Aides et astuces
Education: Autres liens, sites ou portails
 Bibliographie
Bibliographie
Pour citer cette page: (en chimie)
ABROUGUI, M & al, 2020. Solution en chimie. In Didaquest [en ligne]. <http:www.didaquest.org/wiki/Solution_en_chimie>, consulté le 19, mai, 2025
- ..................
- ..................
- ..................
- ..................